随着生物技术的飞速发展,抗体药物在肿瘤、自身免疫性疾病等领域的应用越来越广泛。传统的静脉注射方式需要在医院用药,同时还存在给药时间长、患者依从性低等问题。以曲妥珠单抗为例,传统的静脉输注剂型要求乳腺癌患者每3周前往医院接受一次治疗,每次给药耗时30-90分钟。相比之下,其皮下注射剂型仅需2-5分钟即可完成治疗,这对于需要长期接受抗HER2治疗的患者来说,无疑是一种更加便捷的治疗体验。
因此,抗体药的给药方式在近几年正发生着变革。自2014年以来,随着FDA批准抗体药物数量的增加,皮下制剂的数量也显著增加。截至2024年,FDA批准上市抗体药的给药方式中,皮下注射(SC)是静脉注射(IV)后第二大给药方式,占比超30%。
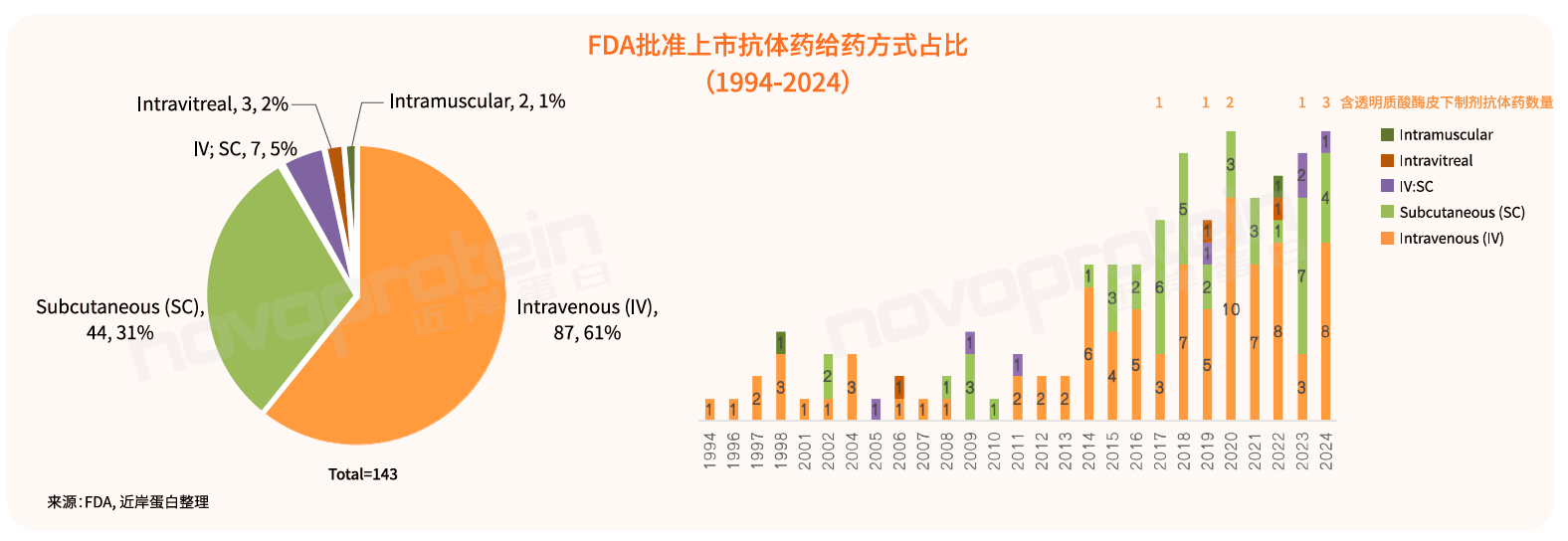
皮下注射(SC)制剂开发的关键难点是给药体积限制所带来的挑战,由于要考虑注射速度、注射部位、个体患者特征(疼痛感觉敏感性)等多方面因素,通常皮下给药最大注射量约为1-2 mL。SC的生物利用度小于静脉(IV)给药,要想和静脉注射制剂达到相同的给药剂量就往往需要制备高浓度的蛋白制剂,而高浓度蛋白溶液则往往会带来稳定性差、高粘度、蛋白溶解度、蛋白降解和聚集等问题。
透明质酸酶皮下制剂抗体药的出现,为行业带来了全新的解决方案。
透明质酸酶是一种能够降解透明质酸(HA)的酶,通过降低细胞间质的粘性,显著增加皮下给药的最大注射量。这不仅使得抗体药物可以通过皮下注射的方式快速进入体内,大大缩短给药时间,同时还可降低给药频率。

截至2024年,FDA已批准8款含透明质酸酶的皮下制剂抗体药上市。利妥昔单抗和曲妥珠单抗的患者用药偏好性调查结果显示[1,2],超75%的患者在静注给药和皮下给药中选择了皮下给药的方式,理由均为更短的给药时间。同时,在已上市注射剂的基础上,进一步开发皮下给药剂型也可以帮助企业通过对新剂型专利的保护进一步延长药物的生命周期。
FDA已批准上市含透明质酸酶的皮下制剂抗体药
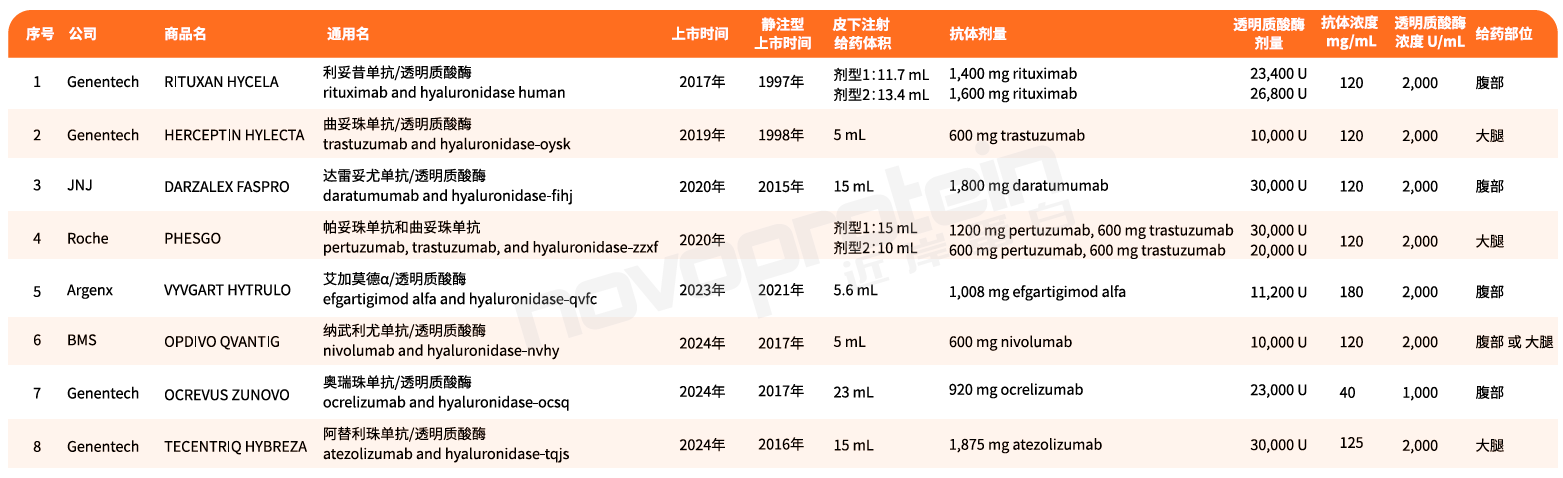
信息来源:药品说明书、近岸蛋白整理
慢性病的治疗一般需要进行长期用药,自身免疫性疾病和心血管疾病作为慢性病,其抗体药物的剂型大多设计为皮下注射剂,部分产品甚至已开发成患者可居家自行注射的笔型制剂,极大提升了用药的便利性。随着更多疗效更优的治疗药物问世,恶性肿瘤的治疗模式也在逐渐向慢性病管理转变。未来,门诊形式的肿瘤免疫治疗将成为常态。抗体药物从传统的静脉注射剂向皮下制剂的转变和优化,正是顺应了这一趋势,为癌症及慢性病患者提供了更加便捷的疾病管理方式,进一步改善患者的生活质量。
杭州九源基因工程股份有限公司(以下简称“九源基因”)与苏州近岸蛋白质科技股份有限公司(以下简称“近岸蛋白”)宣布,双方就重组人透明质酸酶(rHuPH20)达成合作。根据合作协议,近岸蛋白获得九源基因重组人透明质酸酶rHuPH20在大中华区的销售许可。
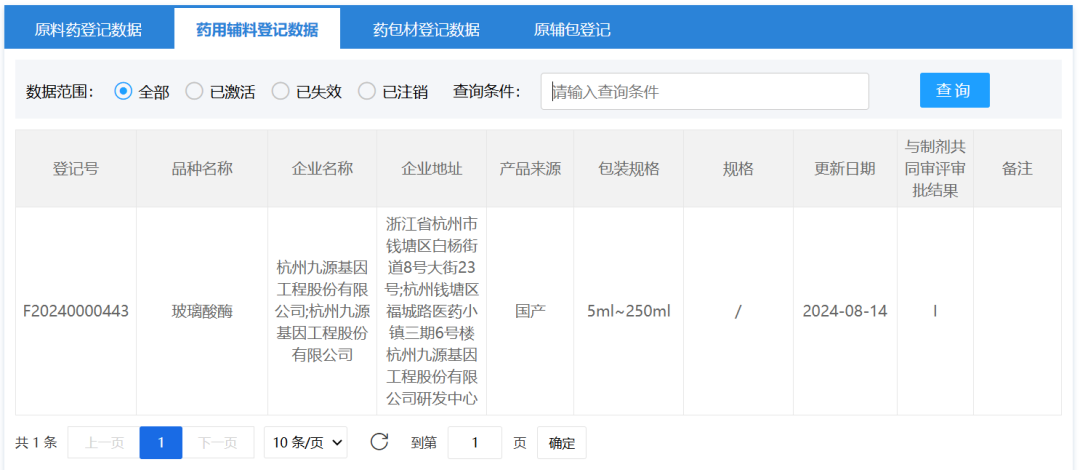
九源基因重组人透明质酸酶已在CDE完成药用辅料登记并公示,登记号为F20240000443。该产品通过基因工程技术获得,并在中国仓鼠卵巢(CHO)细胞中进行表达,在高标准的制备工艺和严格的质量控制下生产,纯度高、活性高,内毒素含量低、稳定性好、批间差异小,且不含动物源成分,无外源性病毒污染。
扫码反馈重组人透明质酸酶需求

产品基本信息

相关支持
如用户计划采用本产品作为药用辅料,近岸蛋白将协助其与生产商共同沟通资质资料、现场审计、长期供货承诺等相关事宜。
资质资料包括但不限于:登记人基本信息、辅料基本信息、生产工艺和过程控制、物料控制、关键步骤和中间体控制、工艺验证和评价、生产工艺的开发、特性鉴定、质量控制、批检验报告、稳定性研究、药理毒理研究等。

杭州九源基因工程股份有限公司玻璃酸酶辅料备案提交资料目录
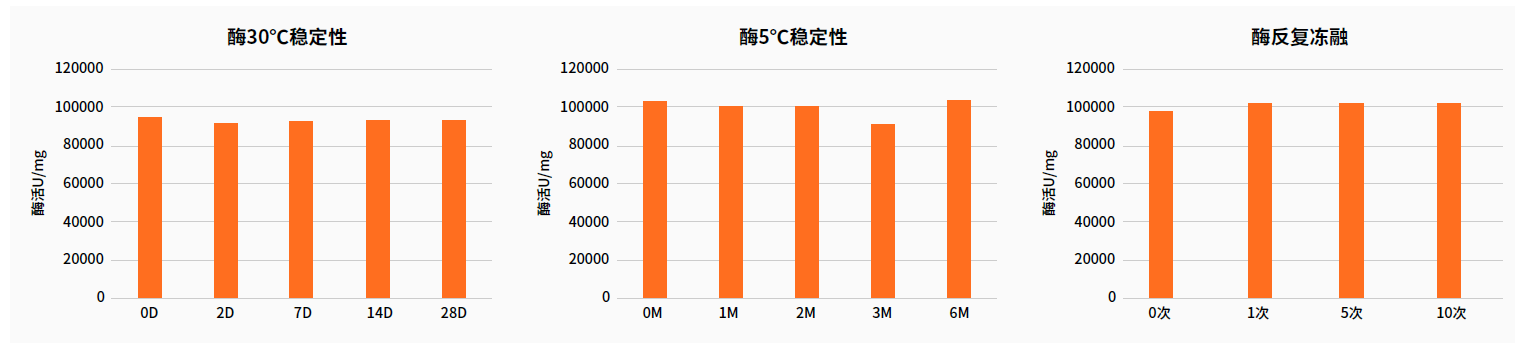
产品稳定性
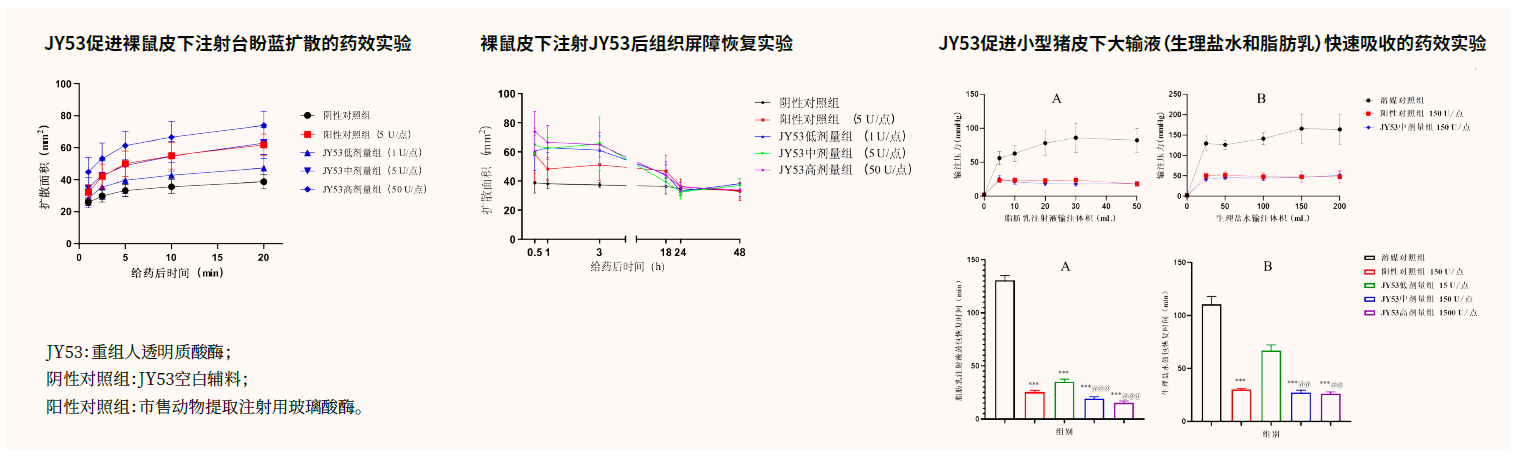
体内生物活性
安全性评估

